
-
0Patients
-
0Hospitals
-
0Studies


Portable and easy-to-use solution
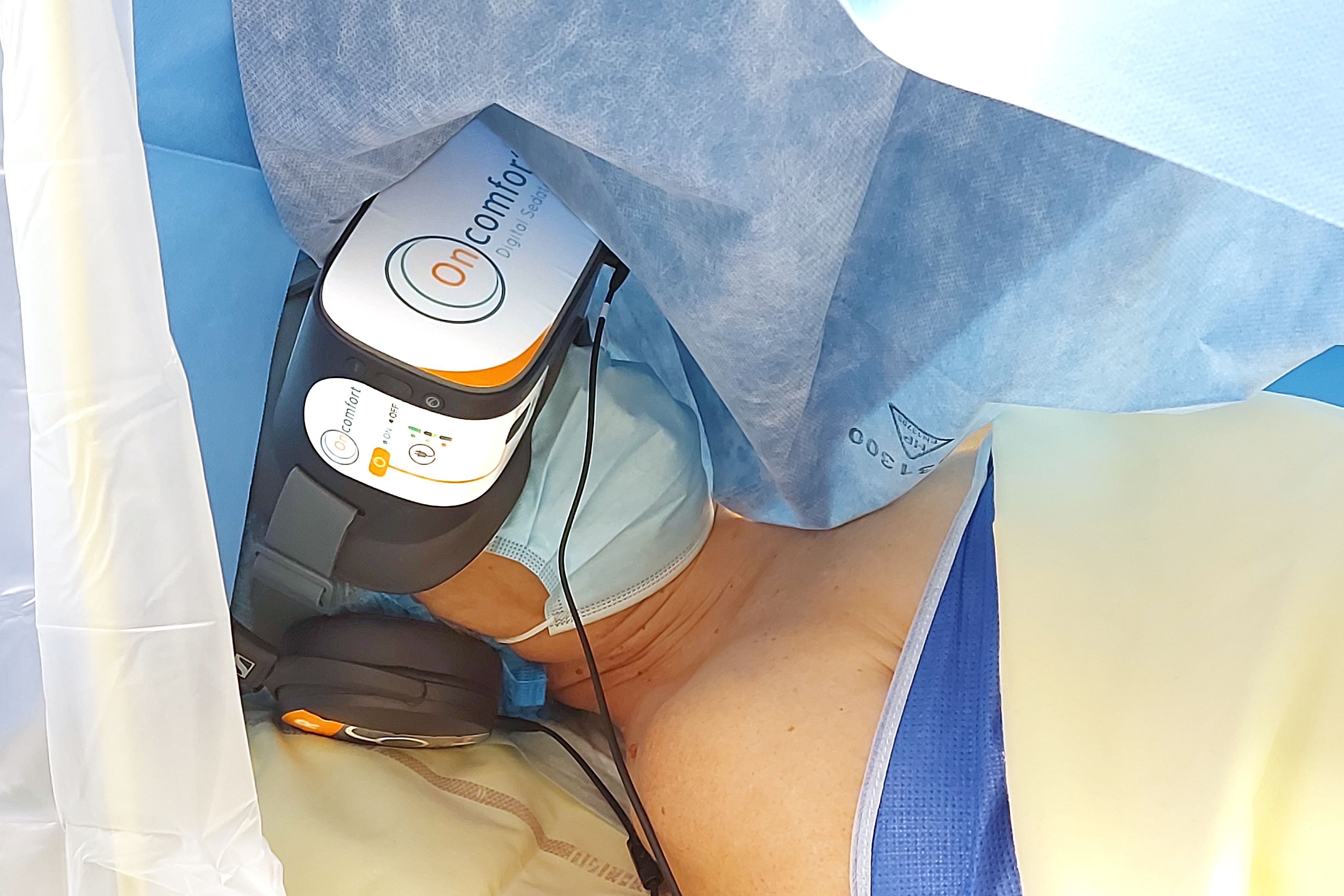
The Oncomfort Sedakit™ is an all-in-one portable solution to deliver Digital Sedation™. The Sedakit™ makes Digital Sedation™ simple, easy and accessible for both adults and children in a wide range of medical interventions. It respects the strict hygiene requirements of a medical environment.
Better outcome - Happier patients
Optimised workflow and better working conditions
The Sedakit™ enables healthcare professionals to better focus on the medical intervention itself. Thanks to Digital Sedation™, the use of medication is significantly reduced which can lead to fewer side effects and improved safety for the patients. The patients are calmer and less anxious with a reduced pain perception. This improves healthcare professionals' working conditions.
Less pain, less anxiety for patients
The Sedakit™ improves patient experience by significantly reducing pain and anxiety. Need for medication is reduced, which can lead to less side effects and faster recovery. Patients are more satisfied and more comfortable throughout their medical journey.
Strategic benefits for medical institutions
Institutions adopting Digital Sedation™ are perceived as more patient-centric and innovative. Healthcare professionals report significantly higher satisfaction rate when using Digital Sedation™. Cost reduction can be achieved through shorter procedure time as well as faster patient recovery.
Medical device with clinically proven effectivity
Digital Sedation™ is effectively replacing intravenous sedation with similar comfort and satisfaction during regional anaesthesia.
Digital Sedation™ is proven to be an adequate substitute for pharmacological sedation and an efficient method to manage pain and anxiety during a patient’s hospital stay. The efficacy has been demonstrated by international clinical studies including more than 2,000 patients.

Meet our
innovative team
Oncomfort is the inventor of and leader in Digital Sedation™.
We are a strong, patient-focused team sharing a common passion for innovation as a driver for better patient care. We thank our talented and renowned partners that have helped us in developing our revolutionising solution.




I started using Digital Sedation™ for the comfort of my patients during breast biopsies. I realised that it not only changed my patients’ experience but also eases my daily work. I am more focused, more efficient, and the interventions are smoother.
V. Mendez, MD, Senologist, CHIREC, Brussels, Belgium
As an interventional radiologist, I perform invasive procedures every single day. We have an anaesthetist in the unit for one day per week. I had no solution to ensure my patients’ comfort on the other days. Digital Sedation™ has now become a must-have in my practice.
F. Cornelis, PHD, Interventional radiologist, APHP, Paris, France